Em um movimento pioneiro para a saúde pública no Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) anunciou nesta segunda-feira (01/04) a aprovação do registro da vacina Abrysvo, desenvolvida pela Pfizer. Este avanço representa um marco significativo na luta contra o vírus sincicial respiratório (VSR), principal causador de infecções respiratórias agudas em bebês, incluindo a bronquiolite.
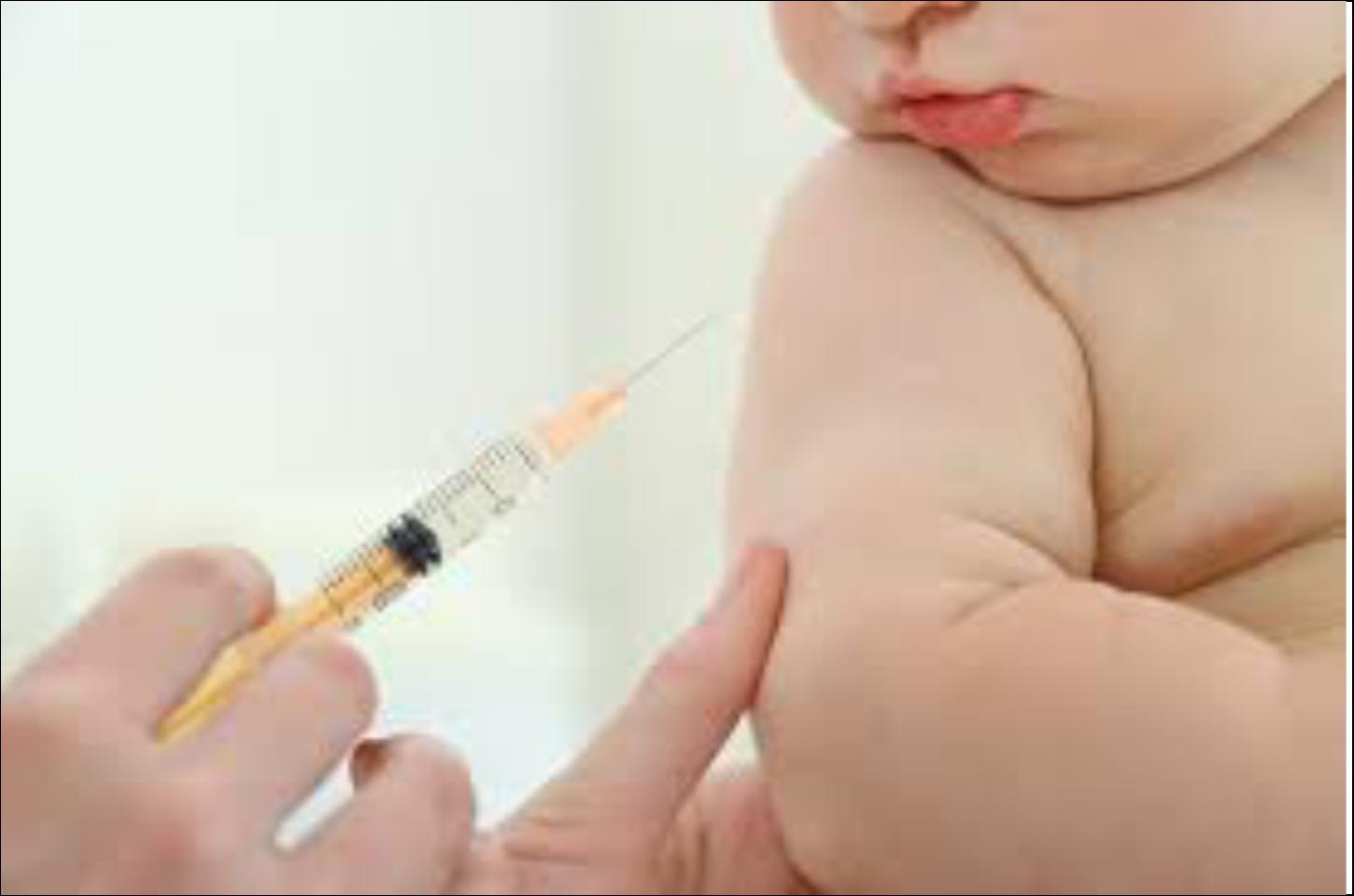
A bronquiolite, uma condição caracterizada pela inflamação dos brônquios, tem sido uma fonte de grande preocupação para pais e profissionais da saúde devido ao seu alto potencial de risco para crianças pequenas e bebês. O imunizante Abrysvo surge como uma solução inovadora, oferecendo proteção desde o nascimento até os 6 meses de idade através da imunização ativa de gestantes. A estratégia de aplicação da vacina durante a gravidez é um passo revolucionário, assegurando que os recém-nascidos estejam protegidos sem a necessidade de serem vacinados diretamente.
Além de focar na proteção infantil, a Anvisa também autorizou o uso da Abrysvo para a prevenção da doença do trato respiratório inferior em adultos com 60 anos ou mais, um grupo também considerado de alto risco para complicações relacionadas ao VSR.
A vacina Abrysvo é classificada como bivalente, pois contém dois antígenos da proteína de superfície F do VSR, requerendo apenas uma dose única aplicada via intramuscular. As gestantes devem receber a vacina durante o segundo ou terceiro trimestre da gestação, oferecendo uma nova camada de segurança para a saúde do bebê antes mesmo de seu nascimento.
Embora tenham sido relatados efeitos colaterais leves, como dor no local da injeção, dor de cabeça e dor muscular, a avaliação geral da Anvisa conclui que os benefícios da vacinação superam significativamente os riscos associados. A eficácia, segurança e qualidade da vacina foram rigorosamente comprovadas, atendendo aos critérios estabelecidos pela Resolução RDC n° 55/2010, que regula o registro de produtos biológicos no país.
Este processo de análise e aprovação da vacina foi priorizado pela Anvisa, dada a sua relevância para a saúde pediátrica, conforme estabelecido no Art. 3º da Resolução RDC n° 204/2017. Esta decisão ressalta o compromisso da agência com a introdução de tratamentos inovadores que atendam às necessidades urgentes de saúde pública, especialmente entre as populações mais vulneráveis.
Anteriormente, a Anvisa já havia aprovado a vacina Arexvy, produzida pela GlaxoSmithKline, destinada à prevenção de doenças causadas pelo VSR, mas com uso restrito a pessoas com mais de 60 anos. Com a aprovação da Abrysvo, abre-se um novo capítulo na proteção contra doenças respiratórias graves, oferecendo esperança a milhares de famílias brasileiras e reforçando o papel vital das vacinas na promoção da saúde pública.
Participe do nosso grupo de WhatsApp e receba notícias com credibilidade ![]()

























 AbdallahNews
AbdallahNews